教学目标
知识目标
1.复习巩固初中四种基本反应类型以及从得氧、失氧角度划分氧化反应和还原反应,使学生进一步了解化学反应的多种分类方法,并由此得出划分的依据不同而有不同的使用范围的结论。
2.使学生理解、掌握用化合价升降的观点和电子转移的观点分析氧化还原反应。
3.使学生了解与氧化还原反应相关的概念及表示方法和意义。
能力目标
通过“讨论式”学习方法的训练,培养学生独立思考及分析,解决问题的能力。
情感目标
培养对立统一的辩证唯物主义的观点。
教材分析
本节内容可分为三部分:化学反应的类型、氧化还原反应、氧化剂和还原剂。重点是氧化还原反应。
化学反应类型,从复习初中的一些化学反应入手,总结归纳四种基本化学反应类型,提出新的化学反应: ![]()
![]()
![]() ,说明初中所学知识不能对它进行分类,从而转入氧化还原反应的教学。
,说明初中所学知识不能对它进行分类,从而转入氧化还原反应的教学。
本节教学重点:用化合价升降和电子转移的观点理解氧化还原反应。
本节教学难点:用化合价升降和电子转移的观点分析氧化还原反应。
教学建议
第一节 氧化还原反应
氧化还原反应的教学建议采用对比法或列表法,教学过程可分为以下四部分(供参考,可根据实际情况进行删减)。
一、有关氧化还原反应的概念
vAlign=top width=157>
实质
vAlign=top width=428 colSpan=2>反应中有电子转移(电子得失或电子偏移)。
原子或离子失电子总数=原子或离子得电子总数
vAlign=top width=157>特征
vAlign=top width=428 colSpan=2>原子或离子化合价升高总数=原子或离子化合价降低总数
vAlign=top width=157>反应
(氧化反应、还原反应)
vAlign=top width=222>反应物中元素(原子或离子)失电子,发生氧化反应(被氧化)
vAlign=top width=206>反应物中元素(原子或离子)得电子,发生还原反应(被还原)
vAlign=top width=157>反应物
(还原剂、氧化剂)
vAlign=top width=222>此反应物(失电子的原子或离子)是还原剂
vAlign=top width=206>此反应物(得电子的原子或离子)是氧化剂
vAlign=top width=157>生成物
(氧化产物、还原产物)
vAlign=top width=222>还原剂被氧化后的生成物叫氧化产物。
vAlign=top width=206>氧化剂被还原后的生成物叫还原产物。
vAlign=top width=157>性质
(还原性、氧化性)
vAlign=top width=222>失电子的性质是还原性,还原剂具有还原性。
vAlign=top width=206>得电子的性质是氧化性,氧化剂具有氧化性
二、常见的氧化剂和还原剂
1.氧化剂
活泼的非金属: ![]() 等。
等。
含有较高化合价元素的化合物: ![]() 、
、 ![]() 、
、 ![]() 、浓
、浓 ![]() 、
、 ![]() 、
、 ![]() 、
、 ![]() 、
、 ![]() 、
、 ![]() 等。
等。
2.还原剂
金属: ![]() 等;
等;
某些非金属: ![]() 等;
等;
含有较低化合价元素的化合物: ![]() 、
、 ![]() 、
、 ![]() 、
、 ![]() 、
、 ![]() 、
、 ![]() 、
、 ![]() 等。
等。
注意:氧化剂和还原剂的确定是以实际反应为依据的,是相对而言的。同一物质处于中间价态的在不同条件,不同反应中,可以作还原剂,也可做氧化剂。
三、氧化还原反应中电子转移的表示方法
1.单线桥法:在氧化剂和还原剂之间表示电子转移关系,在线上标出电子转移总数,箭头指出转移的方向。
例如:
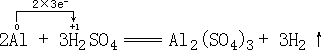
2.双线桥法:此法不仅能表示出电子转移的方向和总数,还能表示出元素化合价升降和氧化、还原关系。双线桥的箭头始于反应物有关元素的原子或离子,箭头指向发生化合价变化后生成物中对应元素的原子或离子。在线上需标明“失去”或“得到”电子总数,化合价的升降以及该元素“被氧化”或“被还原”。例如:

四、四种基本类型反应与氧化还原反应的关系
置换反应都是氧化还原反应;复分解反应都是非氧化还原反应;有单质参加的化合反应和有单质生成的分解反应都是氧化还原反应
教学设计方案
第一节 氧化还原反应
教学目标
知识目标
1.复习巩固初中四种基本反应类型以及从得氧、失氧角度划分氧化反应和还原反应,使学生进一步了解化学反应的多种分类方法,并由此得出划分的依据不同而有不同的使用范围的结论。
2.使学生理解、掌握用化合价升降的观点和电子转移的观点分析氧化还原反应。
3.使学生了解与氧化还原反应相关的概念及表示方法和意义。
能力目标
通过“讨论式”学习方法的训练,培养学生独立思考及分析,解决问题的能力。
情感目标
培养对立统一的辩证唯物主义的观点。
教学重点、难点
重点:用化合价升降和电子转移的观点理解氧化还原反应。
难点:用化合价升降和电子转移的观点分析氧化还原反应,并能灵活运用。
教学方法:复习旧知—创设情境—探索新知—